La Organización Mundial de la Salud informó los primeros días de mayo que a la fecha se han presentado más de 100 vacunas candidatas [1] contra el nuevo coronavirus responsable de la pandemia más severa de las últimas décadas, de las cuales 7 u 8 son las más promisorias ya que son las que probablemente entreguen mejores resultados en cuanto a su capacidad de generar inmunidad de manera preventiva.
Pero “crear” una vacuna no es tan fácil ni tan rápido como decirlo, y hay razones para que así sea. Históricamente, el desarrollo de vacunas ha tomado muchos años, por ejemplo, para la fiebre tifoidea, una enfermedad que alcanzó relevancia en el siglo XIX, fue sino hasta 105 años después que se identificó el agente causante que se logró desarrollar la vacuna capaz de combatir la enfermedad. Para el sarampión el proceso tomó más de 40 años y para el VIH ―virus de inmunodeficiencia humana― van 37 años sin llegar a un resultado exitoso [2] (Figura 1).
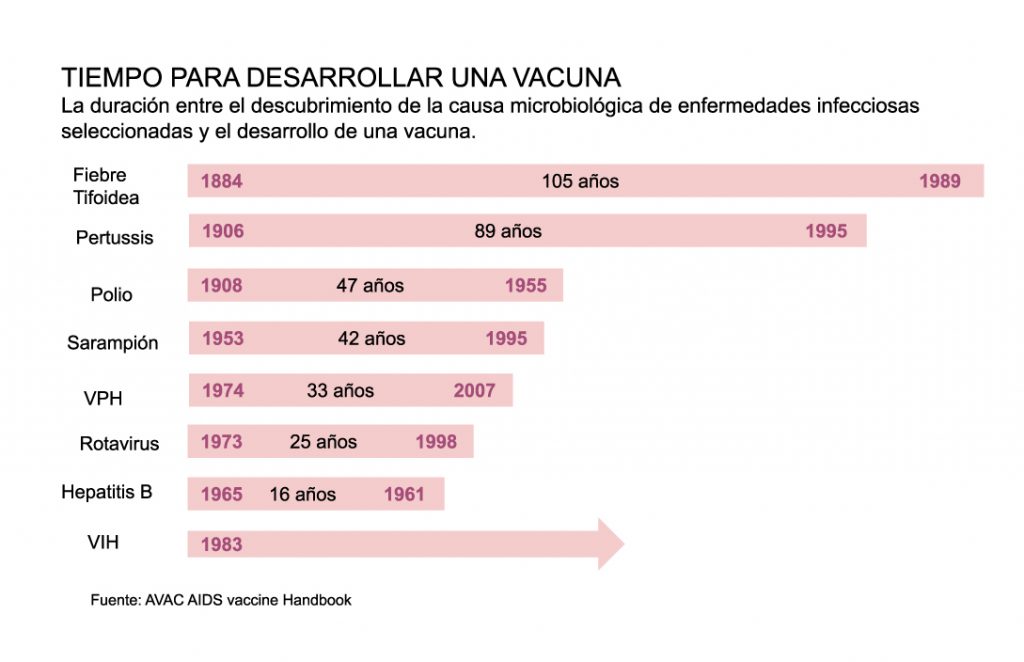
La vacuna para las paperas, considerada ―por ahora― como la más rápida de la historia, demoró 4 años desde la colección de muestras biológicas a la aprobación y licenciamiento en 1967. Esta enfermedad es provocada por un virus de tipo paramixovirus del cual solo se conoce un serotipo [3], hecho que facilitó la rapidez del proceso. Sin embargo, todo indica que la vacuna para COVID-19 llegará para quitarle el trono a la vacuna para las paperas dentro de los próximos meses.

La experiencia chilena
En nuestro país, la vacuna contra el virus respiratorio sincicial en la cual trabaja el equipo de investigación del doctor Alexis Kalergis, director del Instituto Milenio de Inmunología e Inmunoterapia (IMII) de la Pontificia Universidad Católica, comenzaron este esfuerzo el año 2004 y la culminación de este proceso se espera próximamente [4].
Sin embargo, el equipo del Dr. Kalergis es uno de los muchos laboratorios que ha redirigido su trabajo al desarrollo de una vacuna para COVID-19. La vacuna en desarrollo por este grupo consiste en utilizar antígenos o fragmentos de antígenos del coronavirus, una estrategia que escogieron por su capacidad de inducir una respuesta inmune favorable para la eliminación del virus en ausencia de inflamación excesiva.
El uso de antígenos de SARS-CoV-2, que corresponden a moléculas -generalmente proteínas en el exterior de los virus- que son reconocidas de manera específica por el sistema inmune del huésped y desencadenan la defensa, es una estrategia equivalente a la que ya implementó este grupo de investigación en el desarrollo exitoso de la vacuna contra el virus respiratorio sincicial.
Según el Dr. Kalergis, la vacuna chilena podría estar disponible para producirla a gran escala en el plazo mínimo de 2 años, sólo si se cumplen las condiciones en el mejor escenario posible. Recientemente recibieron un aporte financiero de la Fundación Copec-UC para continuar con los ensayos de la vacuna, lo que sin duda significa facilitar el proceso. No obstante, el investigador es sensato en hacer énfasis en que “estos procesos toman tiempo y requieren una serie de estudios preclínicos y clínicos que deben cumplir con regulaciones bastante estrictas” [5], refiriéndose al inicio de pruebas en humanos que se estima para el año 2021.
Tiempos normales contra la urgencia de la pandemia
Actualmente el desarrollo de vacunas sigue siendo un proceso largo, complejo y lineal que tarda en promedio de 10 a 15 años, pero en este caso para COVID-19 se han modificado los plazos normales y se ha adaptado lo que se ha denominado un “desarrollo acelerado”, en donde se acortan los tiempos de investigación y del proceso regulatorio, además de acelerar e incluso superponer las etapas experimentales de ensayos clínicos y preclínicos (Figura 2). Esta adaptación no significa que la seguridad o la calidad del producto final se vean reducidas.
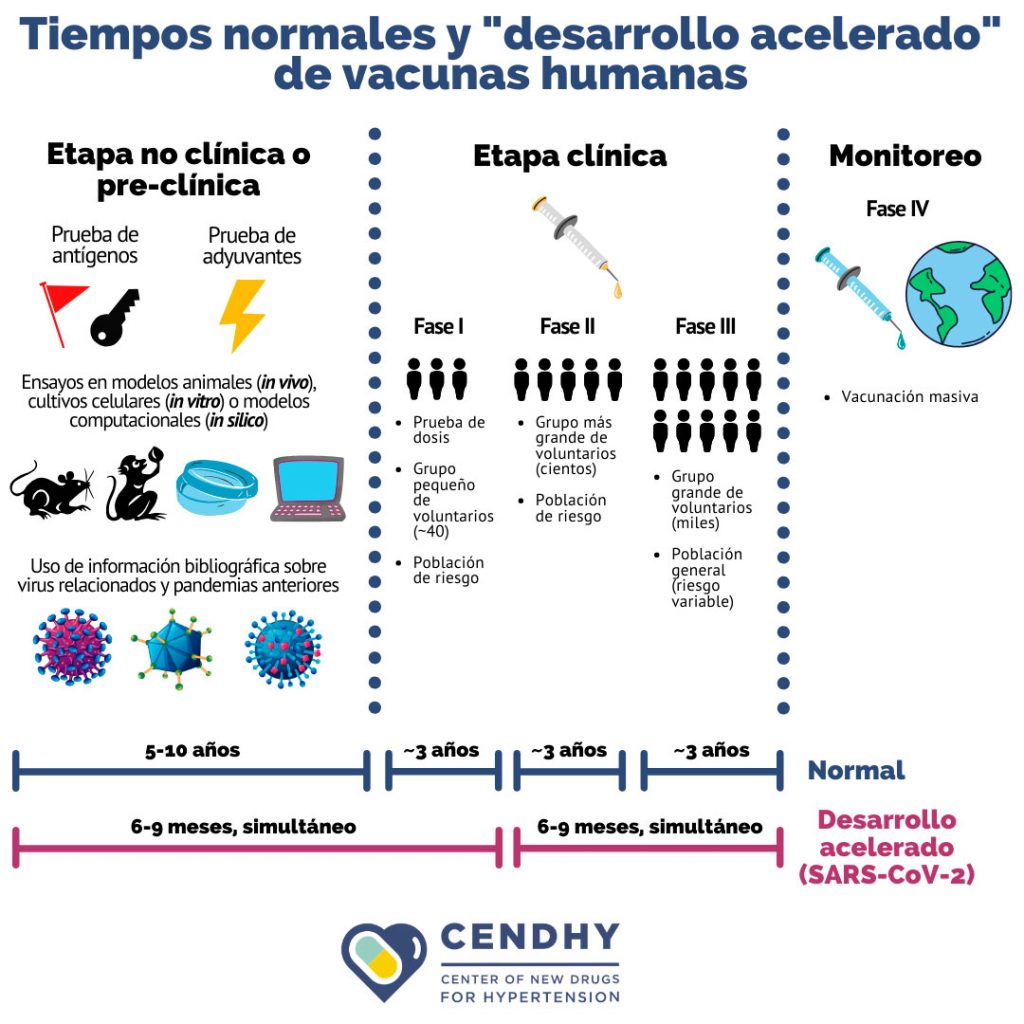
A la par de los esfuerzos por contener lo mejor posible la propagación del virus, como las medidas sanitarias y de confinamiento, cientos ―sino miles― de equipos de investigación científica en el mundo están enfocados en encontrar una vacuna para enfrentar la pandemia e inmunizar a la población. A pesar de que la esperanza de la ciudadanía recae en una vacuna para COVID-19, los investigadores e investigadoras tienen claridad de que el desarrollo de una vacuna no es una carrera de velocidad, sino una verdadera pirámide humana que requiere la cooperación y el compromiso de numerosos actores, y que es igualmente importante ser capaces de garantizar tanto la eficacia como la seguridad de un elemento de prevención tan esperado como esta vacuna.
La urgencia por una pronta solución
A comienzos de junio se registraron 6 millones de casos confirmados positivos para este coronavirus en el mundo, y se han informado más de 371.000 muertes [6], lo que refleja la severidad de la nueva pandemia a la que nos enfrentamos desde el primer caso reportado en la región china de Wuhan en diciembre del 2019 [7].
La enfermedad causada por el nuevo coronavirus, denominado SARS-CoV-2, tiene como nombre COVID-19 y produce síntomas similares a la gripe: fiebre, tos seca, dificultad para respirar, dolor muscular y fatiga [8]. En cuadros graves puede generar neumonía, síndrome de dificultad respiratoria aguda, incluso sepsis ―respuesta exacerbada a una infección― y choque séptico, lo cual conduce a algunos enfermos a la muerte.
¿Por qué una vacuna?
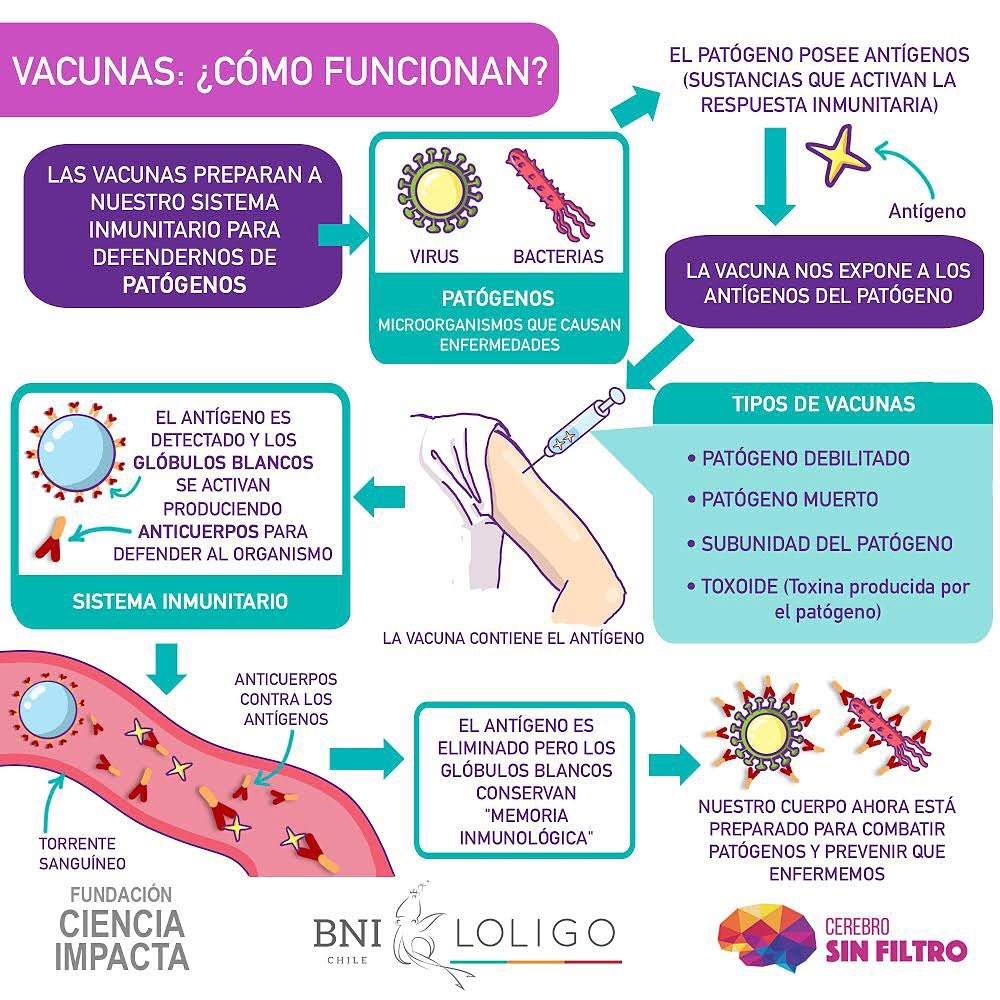
Primero es necesario responder otra pregunta: ¿cómo funciona una vacuna? Y para aclarar esta pregunta, antes debemos abordar ciertos puntos relacionados con el sistema inmune humano, el sistema de defensa de nuestro organismo, que se compone de células especializadas y órganos diversos en nuestro cuerpo.
El objetivo de la vacunación es claro: prevención. Una vacuna simula una infección pero no desencadena la enfermedad, lo que sí genera en el cuerpo es el inicio de la respuesta inmune, por eso se refiere a la vacunación como parte de los programas estatales de inmunización de la población [9]. El sistema inmune humano actúa coordinadamente a través de las respuestas innata y adaptativa, y la vacunación apunta al sistema inmune adaptativo, que “aprende” a reconocer patógenos invasores que le son desconocidos, tal como SARS-CoV-2, de manera de preparar al organismo para un nuevo evento de infección por el mismo patógeno.
Es importante entender que una vacuna no entrega al individuo que la recibe los escudos para protegerse contra la enfermedad, tampoco es un remedio que alivie la enfermedad. El modo en que una vacuna entrega protección es que promueve que el organismo genere ―con su propia materia prima― sus defensas específicas para ese agente infeccioso.
La ruta del coronavirus en el cuerpo humano
Ante la exposición al nuevo coronavirus, nuestro cuerpo no lo logra identificar y “lo deja pasar” libremente a través de diversas vías de entrada: nariz, boca, piel [10] y cualquier epitelio con mucosas que se oriente al exterior. SARS-CoV-2 es un virus cuyo material genético es una hebra individual de ácido ribonucleico (ARN) que, a diferencia de lo que ocurre en células humanas, no se encuentra protegido dentro de un compartimento cerrado como es el núcleo celular. Otra diferencia fundamental es que el material genético del ser humano es una hebra doble de ácido desoxirribonucleico (ADN). A pesar de esta aparente incompatibilidad, este coronavirus es capaz de irrumpir en nuestras células, en los núcleos de nuestras células, en nuestro material genético (ADN) y causar grandes daños.
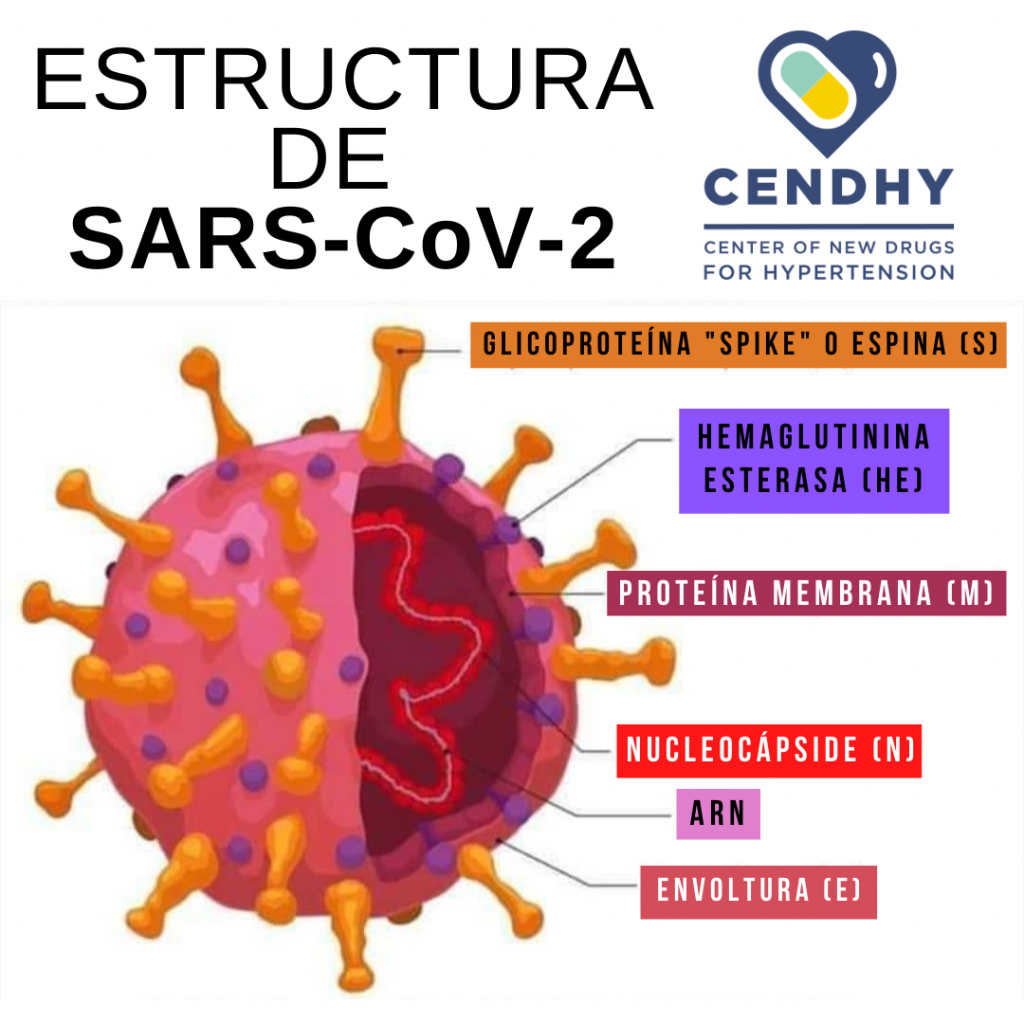
Si bien el ARN de este virus no se encuentra dentro de un núcleo, el coronavirus tiene un límite exterior conocido como envoltura, compuesta principalmente por lípidos y proteínas. Particularmente importantes son la ―a esta altura― famosa proteína spike o “espina”, y la proteína M, ambas orientadas hacia afuera (Figura 3). Estas dos proteínas son las principales responsables de la entrada de SARS-CoV-2 a la circulación, ya que el virus se une a la Enzima Convertidora de Angiotensina II (ACE2) en la superficie de las células humanas en numerosos órganos del cuerpo, como pulmones, riñones y corazón, e ingresa sin mucho problema.
Frecuentemente se describe este proceso de reconocimiento, unión y anclaje de ligandos con sus receptores mediante el “modelo de llave y cerradura” (“Lock and key” [11]), donde la llave es una de las proteínas del virus, en este caso la proteína espina, y la cerradura es la proteína de superficie, el receptor ACE2, que permite su acceso a las células (Figura 4).
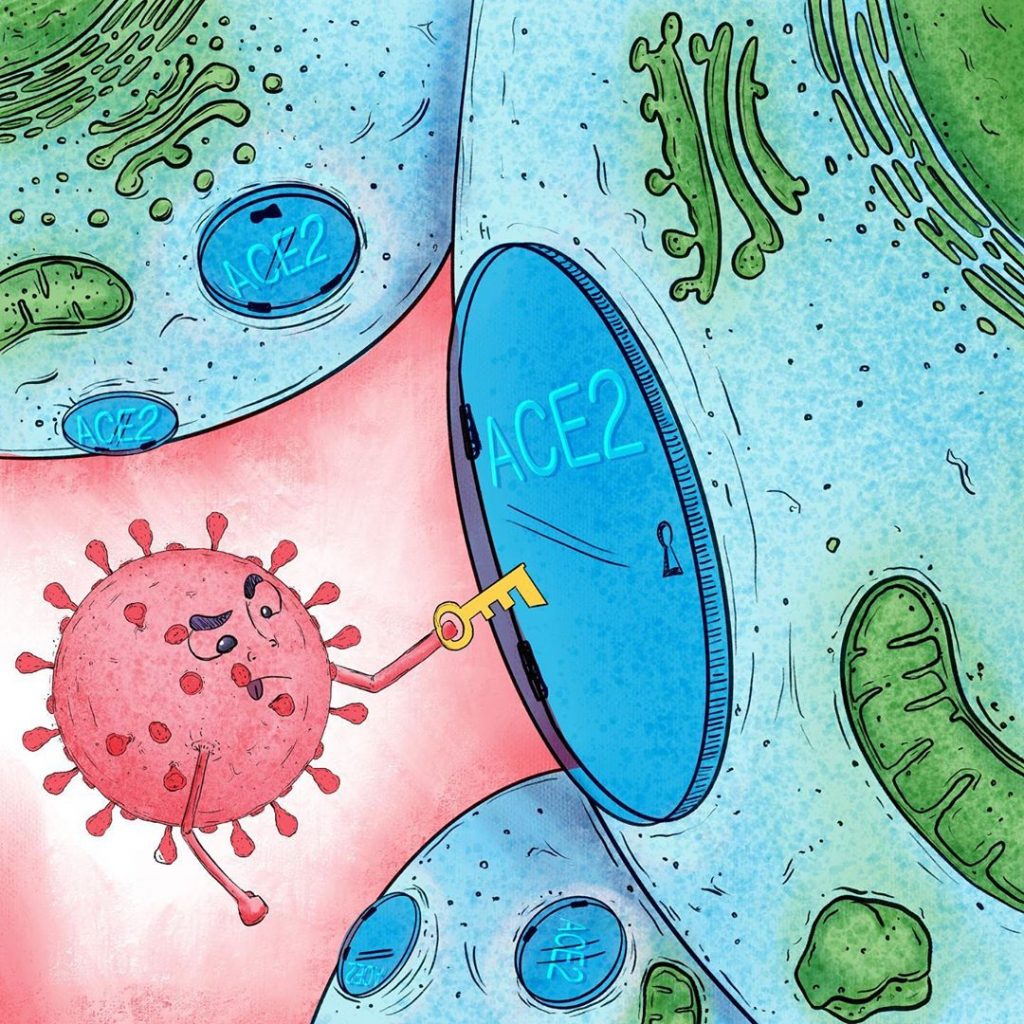
Una vez dentro de una célula humana, el coronavirus toma control de todas las herramientas disponibles y comienza a producir más partículas virales, clones de sí mismo, y a infectar tanto células cercanas como distantes. Se da inicio a la respuesta inmune cuando un tipo especializado de células, las Células Presentadoras de Antígenos (APC por sus siglas en inglés “Antigen Presenting Cells”), envuelven al virus y exponen en su propia superficie algunos fragmentos importantes de este para “llamar la atención” de otras células del sistema inmune y de esta manera activarlas, por eso se dice que las “presentan”.
Estas células a las que “llaman” las APC son las “células T colaboradoras”, que a su vez permiten que se dé inicio a otras ramas de la respuesta inmune: las células B o linfocitos B producen anticuerpos que evitan que el virus infecte a más células humanas, así como también “marcan” al virus para que sea reconocido como objetivo de destrucción. Gracias a esta marca, las “células T citotóxicas” identifican a las células infectadas por el virus y las eliminan, de ahí su nombre: “tóxicas para las células” (Figura 5). Así es, de manera simplificada, es cómo se lleva a cabo la respuesta inmunitaria frente a un agente infeccioso nuevo o desconocido.

Vacunación y memoria inmunológica
La vacunación imita una infección ya que emplea estos elementos importantes del virus, que mencionamos anteriormente, que “llaman la atención” de células del sistema inmune, las activan y estas desencadenan el inicio de la respuesta inmunitaria. La diferencia fundamental es que esta imitación es de forma controlada y no genera la enfermedad, sin embargo, una vez que la imitación de la infección “desaparece”, el cuerpo se queda con una reserva de linfocitos de memoria que “recordarán” cómo combatir la enfermedad en el caso eventual de que en el futuro se vuelva a encontrar con el mismo agente infeccioso, lo que se conoce como memoria inmunológica (Figura 6). Esta memoria es específica y puede durar varios años, se reactiva cada vez que el organismo se ve nuevamente enfrentado al mismo patógeno.
Desarrollo de vacunas: “ni tan fácil, ni tan rápido”
Para desarrollar una vacuna primero se debe identificar el agente microbiológico que causa la enfermedad, estudiarlo, caracterizarlo, y luego investigar los antígenos que serán útiles para una posible vacuna. Un antígeno es uno de estos “elementos importantes que llaman la atención de células del sistema inmune, las activan y estas desencadenan el inicio de la respuesta inmunitaria” a los que nos hemos referido. La definición técnica de antígeno es “cualquier sustancia que activa la respuesta inmunitaria” [12].
Todas las vacunas tienen como fin el exponer a nuestro cuerpo un antígeno que no causará la enfermedad, pero provocará una respuesta inmune que bloqueará o eliminará al patógeno si la persona se infecta una próxima vez. La presentación del antígeno es el hito que desencadena la respuesta inmunitaria.
Posterior a la etapa de investigación y desarrollo en el proceso por crear una nueva vacuna, se deben revisar detalles como su normativa, para luego fabricar a pequeña escala con el control de calidad correspondiente. El siguiente paso son los ensayos preclínicos en modelos animales (in vivo) para comprobar que efectivamente se produzca una reacción inmunológica y que la vacuna no sea perjudicial, para finalmente comenzar los ensayos clínicos que constan de 4 etapas consecutivas: I, II, III y IV, en las que se prueban las vacunas en humanos.
Cada etapa debe ser debidamente superada y certificada para avanzar a la siguiente, por eso el proceso total de desarrollo de una vacuna es extenso en tiempo, complejo por las múltiples instancias de control, y lineal en donde las etapas son consecutivas y siguen un orden protocolar establecido para cualquier fabricante.
“La vacuna más rápida de la historia”
De las cerca de 100 propuestas de vacunas en desarrollo contra SARS-CoV-2 por equipos de investigación en compañías privadas, centros de investigación, universidades y laboratorios a través del mundo, los investigadores han estudiado diferentes técnicas, algunas de las cuales no se han usado en vacunas autorizadas en el pasado.
Al menos nueve grupos ya han comenzado ensayos de seguridad en humanos según los registros de la OMS, poniendo a prueba formulaciones de vacunas inyectables, mientras que otros se encuentran en las pruebas en modelos animales. Es importante destacar que las compañías “en carrera” han acelerado el proceso de desarrollo de vacunas de diferentes formas: haciendo pruebas en varios modelos animales a la vez, y en paralelo con pruebas en grupos pequeños de personas. Usualmente el proceso es comenzar en modelos animales y con esos resultados se avanza a los ensayos en humanos, para garantizar que se obtenga respuesta inmunológica cuantificable y que los efectos secundarios sean mínimos. Por esta razón los investigadores reconocen que la falta de tiempo conlleva mayor riesgo [13].
No obstante, dado que los estudios han demostrado que SARS-CoV-2 no muta tan rápido como otros virus como el de la influenza o el VIH, se tiene la confianza de que una vacuna, una vez desarrollada, pueda ser efectiva y entregar protección por bastante tiempo [14]. Dado que el desarrollo de una vacuna para COVID-19 ha tomado el camino del “desarrollo acelerado” (Figura 2), Dan Barouch, director de Virología e Investigación de Vacunas en el Beth Israel Deaconess Medical Center de Boston, profesor de la Escuela de Medicina de la Universidad de Harvard, y líder de uno de los laboratorios que se encuentra trabajando en una vacuna para COVID-19, señala que según las predicciones de la industria a comienzos del año 2021 se podría contar con una vacuna de emergencia o para uso compasivo.
Barouch recuerda que la vacuna para ébola, que también suscitó una emergencia, demoró 5 años en llegar a la población [15]. Una eventual vacuna para COVID-19 se espera en el plazo de un año, por lo que el investigador concluye que “será el desarrollo de una vacuna más rápido de la historia” [16].
Dentro de los casos más conocidos y calificados como prometedores están las empresas Moderna Therapeutics en Cambridge, Massachusetts, e Inovio Pharmaceuticals en Pennsylvania, ambas en Estados Unidos, que se encuentran realizando ensayos preclínicos y clínicos en paralelo.
Moderna anunció el 18 de mayo que los ensayos en humanos de la fase 1 arrojaron resultados promisorios, sin embargo, es importante analizar este tipo de noticias de manera crítica. La compañía informó que la prueba consistió en inocular a solo 8 voluntarios sanos y medir su respuesta inmune a través de la producción de anticuerpos, lo que expertos en inmunología califican como insuficiente para garantizar la efectividad [17]. Con estos resultados, y en conjunto con el U.S. National Institute of Allergy and Infectious Diseases, Moderna avanzó a la fase 2 de sus ensayos.
La vacuna en desarrollo en el Reino Unido que lidera la Universidad de Oxford y la empresa AstraZeneca, encargada del licenciamiento, recibió cerca de 1.2 billones de dólares de parte del gobierno estadounidense [18] y está siendo comprometida para septiembre de este año [19]. Así mismo, la compañía estadounidense Novavax se encuentra realizando ensayos clínicos para la vacuna contra COVID-19 en Australia, y recibió un sustantivo aporte de 388 millones de dólares de parte de una iniciativa sin fines de lucro fundada por Bill Gates [20]. Esta vacuna, de ser aprobada, tendría un pedacito de Chile ya que actualmente sus desarrolladores están investigando el uso de saponina, una sustancia de estructura similar al jabón que produce el árbol del Quillay, nativo de nuestro país, como componente indispensable del potenciador de la vacuna, llamado “Matrix-M” [21].
No es una carrera de velocidad
Si bien se necesita una solución rápida, la urgencia no puede comprometer la seguridad y la salud de las personas. Las analogías de “la carrera por la vacuna contra coronavirus” excluyen un aspecto inherente de la labor científica, que es la comprobación de una hipótesis a partir de los resultados concretos, que surgen de experimentar de manera exhaustiva, racional y justificada.
El protocolo de desarrollo acelerado asegura no comprometer la eficacia, la seguridad, ni la calidad del producto final que es una vacuna. La adaptación de los tiempos normales de desarrollo expone otro aspecto propio de la investigación científica: no es un ejercicio individual, sino que requiere la comunicación, cooperación y coordinación entre personas, instituciones y países. Sólo de esta manera ha sido posible reformular el desarrollo de una vacuna para COVID-19 y ofrecer una solución en tiempo récord.
El desarrollo de una vacuna no es una carrera de velocidad, es más bien un deporte en equipo o una pirámide humana, en que cada nivel y cada bloque son imprescindibles para construir la pirámide completa, desde la base hasta la cima.
No todas las vacunas son iguales
Actualmente numerosos equipos humanos coordinados y distribuidos en todo el mundo se encuentran probando al menos 8 tipos de vacunas para el nuevo coronavirus SARS-CoV-2. Dentro de los tipos de vacunas en las cuales se trabaja, estas utilizan diferentes aproximaciones para cumplir un mismo fin: en algunos casos usan el virus íntegro y en otros utilizan partes del virus para activar la respuesta inmune (Figura 7).

Según la prensa y en palabras de los propios investigadores, las vacunas que “llevan la delantera” en esta metáfora de la carrera de velocidad son básicamente las que están más adelantadas y han presentado resultados preliminares en sus ensayos en humanos. Entre ellas se incluyen la candidata de Moderna Therapeutics que es de tipo viral de ARN; la propuesta conjunta entre la farmacéutica Pfizer y la compañía BioNTech que también es basada en ARN; mientras que la estrategia escogida por la empresa Inovio Pharmaceuticals es basada en ADN [23], al igual que la Universidad de Harvard que trabaja en asociación con Janssen Pharmaceutical de la multinacional Johnson & Johnson [24]. La última contendiente originada desde Estados Unidos es la propuesta por la compañía biotecnológica Novavax y financiada en parte por Bill Gates.
La anticipada promesa inglesa de la Universidad de Oxford y AstraZeneca sería de tipo recombinante, como lo es la vacuna para el ébola. De esta misma naturaleza es la vacuna en desarrollo en la empresa CanSino Biologics, en China. Su competencia local directa son 3 vacunas de tipo viral que emplean a SARS-CoV-2 inactivado, y se encuentran en desarrollo en el Wuhan Institute of Biological Products, el Beijing Institute of Biological Products y la farmacéutica Sinovac Biotech. Desde esta última, los líderes de la investigación aseguraron a finales de mayo que su vacuna CoronaVac tiene un 99% de posibilidades de ser exitosa [25] luego de superar los ensayos en monos y avanzar a la segunda etapa con más de 1000 voluntarios humanos.
Según la actualización más reciente, se informa de 10 candidatas en etapa clínica [26], en su mayoría realizando las fases 1 y 2 en paralelo (Figura 8).

La necesidad por sobre la incerteza
Para concluir, es importante entender que se pueden desarrollar vacunas mediante distintas técnicas, pero el fin es el mismo: lograr crear una vacuna capaz de generar inmunidad en la población para enfrentar esta pandemia. A pesar de que este proceso normalmente puede tomar más de 10 años, en este caso de urgencia para doblegar a COVID-19, se están acelerando etapas, tanto experimentales como regulatorias.
Con procesos acelerados como estos es normal que surjan dudas y desconfianza: ¿es segura?, ¿cuándo va a llegar la vacuna?, ¿necesito vacunarme si tuve la enfermedad?, ¿quién queda inmune?, ¿puedo volver a contagiarme o contagiar?. Luego de una revisión de estudios sobre resfriados comunes algunos investigadores asumieron en un principio que los recuperados por la infección con SARS-CoV-2 pueden mantenerse protegidos de una reinfección por cierto período de tiempo, lo que los cataloga como “inmunes”. Respecto a estas suposiciones, Michael Diamond, inmunólogo viral de la Universidad de Washington en Missouri, Estados Unidos, establece que deben ser “respaldadas por evidencia”. Diamond también expresa que “no sabemos mucho sobre la inmunidad de este virus en particular” [14], frente a lo cual se debe tener cautela y paciencia hasta obtener certezas.
Otra de las preocupaciones más frecuentes es sobre cuánto duraría la inmunidad otorgada por la vacuna. Según Stanley Perlman, virólogo especializado en coronavirus de la Universidad de Iowa: “no se tiene buena evidencia que indique una inmunidad duradera”. Como respuesta a esta interrogante, Diamond espera que se pueda conocer más sobre la infección en estudios en animales y humanos, y que “quizás esta manera acelerada de desarrollar una vacuna no sea la más eficiente pero puede ser la más conveniente” [14].
La necesidad inmediata es prevenir más muertes y cuadros graves de la enfermedad, detener el ascenso de la curva de contagio y proteger a la población, y frente a eso la decisión consenso entre expertos desde diversas áreas científicas, especialistas médicos y autoridades de salud pública, es el actuar de manera inteligente respecto a las incertezas, optando por el desarrollo acelerado de vacunas en un contexto de colaboración interdisciplinaria.
Autores:
Victoria Aguayo, tesista en Drug Delivery Lab y estudiante de Bioquímica, Universidad de Chile.
Lorena Díaz Hemard, Coordinadora científica y de comunicaciones en CENDHY. Ingeniera en Biotecnología Molecular, Universidad de Chile.
Javier Morales Montecinos, PhD. Director e investigador titular en CENDHY. Director de Drug Delivery Lab y académico Universidad de Chile.
Referencias:
[1] Panorama de candidatos para la vacuna de COVID-19 (en inglés) [2 de junio 2020]. World Health Organization (WHO). Disponible en línea: https://www.who.int/who-documents-detail/draft-landscape-of-covid-19-candidate-vaccines
[2] Manual sobre la vacuna del SIDA (en inglés). AVAC, Segunda Edición: “Perspectivas Globales”, 2005. Disponible en línea: https://www.avac.org/resource/aids-vaccine-handbook-2nd-edition-global-perspectives
[3] Vacuna para paperas (en inglés). WHO, actualizado en 2011. Disponible en línea: https://www.who.int/biologicals/vaccines/mumps/en/
[4] “Investigadores UC lideran desarrollo de vacuna chilena contra el coronavirus” (3 de marzo, 2020). Noticias online Pontificia Universidad Católica de Chile. Disponible en: https://www.uc.cl/noticias/investigadores-uc-lideran-desarrollo-de-vacuna-chilena-contra-el-coronavirus/
[5] “Prometedora vacuna chilena contra el coronavirus inicia pruebas pre clínicas” (21 de mayo, 2020). Revista Qué Pasa de La Tercera. Disponible en línea: https://www.latercera.com/que-pasa/noticia/prometedora-vacuna-chilena-contra-el-coronavirus-inicia-pruebas-pre-clinicas/GR67EPSCMRE6VHVNISADFA47ZY/
[6] Estadísticas en tiempo real COVID-19. Worldometers: https://www.worldometers.info/coronavirus/
[7] Reporte de situación N°1: Nuevo Coronavirus (2019-nCoV), 21 de enero (en inglés) [21 de enero, 2020]. WHO. Disponible en línea: https://www.who.int/docs/default-source/coronaviruse/situation-reports/20200121-sitrep-1-2019-ncov.pdf?sfvrsn=20a99c10_4
[8] Plan de Acción Nuevo Coronavirus COVID-19, Ministerio de Salud. Disponible en línea: https://www.minsal.cl/nuevo-coronavirus-2019-ncov/
[9] Programa Nacional de Inmunizaciones, Ministerio de Salud. Disponible en línea: https://www.minsal.cl/programa-nacional-de-inmunizaciones/
[10] Hoffmann et al. (2020). SARS-CoV-2 Cell Entry Depends on ACE2 and TMPRSS2 and Is Blocked by a Clinically Proven Protease Inhibitor. Cell Vol. 181, pág.: 271–280. Disponible en línea (PDF): https://doi.org/10.1016/j.cell.2020.02.052.
[11] Tripathi A, Bankaitis VA (2017). Molecular Docking: From Lock and Key to Combination Lock. Journal of Molecular Medicine and Clinical Applications Vol. 2(1). DOI: http://dx.doi.org/10.16966/2575-0305.106 (disponible en línea).
[12] Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter (2002). Molecular Biology of the Cell. Garland Science, 4ta edición.
[13] Callaway, E. (18 de marzo, 2020). Coronavirus vaccines: five key questions as trials begin. Nature, 579(7800), 481. Disponible en línea: https://www.nature.com/articles/d41586-020-00798-8
[14] Callaway, E. (28 de abril, 2020). The race for coronavirus vaccines: a graphical guide. Nature, 580(7805), 576. Disponible en línea: https://www.nature.com/articles/d41586-020-01221-y
[15] Julie E. Ledgerwood et al. (2017). Chimpanzee Adenovirus Vector Ebola Vaccine. New England Journal of Medicine Vol. 376: 928-38. DOI: 10.1056/NEJMoa1410863. Disponible en línea (PDF): https://www.nejm.org/doi/pdf/10.1056/NEJMoa1410863
[16] Charles Schmidt (2020). Genetic Engineering Could Make a COVID-19 Vaccine in Months Rather Than Years. Scientific American June 2020 Issue. Disponible en línea: https://www.scientificamerican.com/article/genetic-engineering-could-make-a-covid-19-vaccine-in-months-rather-than-years1/
[17] Nsikan Akpan (29 de mayo, 2020). A COVID-19 vaccine has passed its first human trial. But is it the frontrunner? National Geographic Science Coronavirus coverage. Disponible en línea: https://www.nationalgeographic.com/science/2020/05/coronavirus-vaccine-passes-first-human-trial-but-is-it-frontrunner-cvd/
[18] David D. Kirkpatrick (3 de junio, 2020). $1.2 Billion From U.S. to Drugmaker to Pursue Coronavirus Vaccine. The New York Times. Disponible en línea: https://www.nytimes.com/2020/05/21/health/coronavirus-vaccine-astrazeneca.html
[19] Coronavirus: AstraZeneca ready to supply potential vaccine in September (21 de mayo, 2020). BBC News. Disponible en línea: https://www.bbc.com/news/business-52751661
[20] Sissi Cao (26 de mayo, 2020). Bill Gates Funds a Crucial COVID-19 Vaccine Human Trial, Merck Adds 2 Candidates. Observer. Disponible en línea: https://observer.com/2020/05/coronavirus-vaccine-update-novavax-merck-bill-gates-funding/
[21] Quillay: El árbol nativo de Chile con el que se están fabricando vacunas contra el COVID-19 (28 de mayo, 2020). Futuro 360. Disponible en línea: https://www.futuro360.com/data/quillay-arbol-nativo-chile-fabricando-vacunas-contra-covid-19_20200528/
[22] Tipos de coronavirus humanos (2020). National Center for Immunization and Respiratory Diseases (NCIRD), Division of Viral Diseases. Centers for Disease Control and Prevention. Actualizado al 15 de febrero, 2020. Disponible en línea: https://www.cdc.gov/coronavirus/types.html
[23] Olivia Willis (23 de mayo, 2020). Who’s leading the race? A guide to coronavirus vaccines in the pipeline. ABC Health & Wellbeing. Disponible en línea: https://www.abc.net.au/news/health/2020-05-24/coronavirus-vaccine-race/12277558
[24] Global race to a COVID-19 vaccine (abril 2020). Harvard News. Disponible en línea: https://news.harvard.edu/gazette/story/2020/04/harvards-coronavirus-vaccine-efforts/
[25] Farmacéutica asegura que hay un 99% de posibilidades de que su vacuna contra el coronavirus funcione (29 de mayo, 2020). Meganoticias. Disponible en línea: https://www.meganoticias.cl/calidad-de-vida/303205-vacuna-coronavirus-exito-sinovac-farmaceutica-china-1yz.html [26] Mullard, A (2020). COVID-19 vaccine development pipeline gears up. The Lancet, Vol. 395(10239), p: 1751-1752. Disponible en línea (PDF): https://doi.org/10.1016/S0140-6736(20)31252-6


0 comentarios